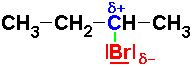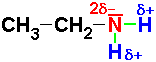Exercice 15B.
Exercice sans calculatrice
Enoncé
Pour chacune des molécules suivantes, repérer les liaisons polarisées, les sites donneurs d'électrons et les sites accepteurs d'électrons.
a) La molécule d'eau.
b) La molécule de propène.
c) La molécule de 2-Bromobutane.
d) La molécule d'éthylamine.
Solution
Dans les réponses ci-dessous, les liaisons polarisées sont représentées en vert, les sites donneurs d'électrons sont en rouge et les sites accepteurs d'électrons sont en bleu.
a) La molécule d'eau : . .
Les liaisons O-H sont polarisées.
L'atome d'oxygène est un site donneurs d'électrons à cause de ses 2 doublets non liants.
Les atomes d'hydrogène sont des sites accepteurs d'électrons à cause de la polarisation des liaisons O-H.
b) La molécule de propène : . .
Les liaisons ne sont pas polarisées (la différence d'électronégativité entre les atomes étant trop petite).
La liaison double est un site donneur d'électrons parce qu'elle peut s'ouvrir facilement.
c) La molécule de 2-Bromobutane : . .
La liaison C-Br est polarisée.
L'atome de brome est un site donneur d'électrons à cause de ses 3 doublets non liants.
L'atome (bleu) de carbone est un site accepteur d'électrons à cause de la polarisation des liaisons C-Br.
d) La molécule d'éthylamine : . .
Les liaisons N-H sont polarisées.
L'atome d'azote est un site donneur d'électrons à cause de son doublet non liant.
Les atomes d'hydrogène sont des sites accepteurs d'électrons à cause de la polarisation des liaisons N-H.